سیستم های رباتیک جراحی های استریوتاکتیک پیچیده را تسهیل می کنند

خلاصه مقاله
سیستم های رباتیک جراحی های استریوتاکتیک پیچیده را تسهیل می کنند
#خبرنامه
#ربات_جراحی_استریوتاکتیک
سیستم های رباتیک جراحی های استریوتاکتیک پیچیده را تسهیل می کنند:
🔰دارای تخصص و فناوری مورد نیاز برای انجام جراحی های عصبی_عملکردی پیچیده است. یک سیستم روباتیک، که در سه بخش اصلی استاندارد شده است، می تواند دقت و کارایی این روش ها را افزایش دهد.
🔰دکتر Junathan J.Parker جراح اعصاب در آریزونا می گوید : سیستم های رباتیک دگرگون کننده هستند. این به ما اجازه می دهد تا با موارد چالش برانگیز صرع و اختلال حرکتی که به کاشت پیچیده الکترود نیاز دارد مقابله کنیم.
این سیستم ها می توانند برای انجام چندین نوع جراحی مغز و اعصاب عملکردی، از جمله تخریب با لیزر ، کاشت الکترود برای تحریک عمیق مغز و تحریک عصبی پاسخگو مورد استفاده قرار گیرد. علاوه بر صرع، شرایط خاصی که می توان با سیستم رباتیک مدیریت کرد شامل لرزش اساسی، بیماری پارکینسون، دیستونی، تومورها و نکروز پرتویی است.
دکترJamie J. Van Gompel, M.D. از جراحان myoclinic میگوید : به عنوان یک شرکت، ما شلوغ ترین برنامه تحریک مغز را در ایالات متحده داریم.
سیستم رباتیک به ما امکان می دهد کاشت های گسترده ای را انجام دهیم که درمان ها را متناسب با نیازهای بیمار انجام می دهد.
🔰یک بازوی فوق پایدار :
متخصصان کلینیک مایو به طور معمول جراحی مغز و اعصاب عملکردی پیچیده ای را انجام می دهند که شامل تعدیل چندین مکان در مغز به طور همزمان است.
🔰دکتر پارکر میگوید: «انجام این کار بدون سیستم رباتیک میتواند از نظر فنی دشوار باشد. زمانی که اعداد به صورت دستی روی فریم های سر استریوتاکتیک تنظیم می شوند، ممکن است خطاهای اندازه گیری رخ دهد. سیستم های رباتیک از این پتانسیل خطای انسانی جلوگیری می کنند.)
🔰این سیستم روباتیک به جراحان مغز و اعصاب کمک می کند تا الکترودها را به طور دقیق قرار دهند و در عین حال از رگ های خونی اجتناب کنند. دکتر سانجیت اس. گروال، جراح مغز و اعصاب در myoclinicدر جکسونویل، فلوریدا، می گوید: این نه تنها خطای هدف، بلکه خطای نقطه ورود را نیز به حداقل می رساند.
این سیستم رباتیک دقت را حتی در مناطقی از مغز که رویکرد جراحی چالش برانگیز است، افزایش می دهد.
🔰دکتر Kai J. Miller جراح myoclinic میگوید :
این ربات به ما اجازه میدهد تا ابلیشنهای لیزری را با دقت بیشتری برای درمانهایی که شامل مسیرهای متعدد در زمانی که ساختارهای نازکی در اعماق مغز را برای جراحی صرع هدف قرار میدهیم، کانتور کنیم.
ما قادر خواهیم بود بالاترین سطح دقت را حفظ کنیم رویکردهایی که با تکنیکهای موجود ما امکانپذیر نبودهاند. این به ویژه با جراحی هایی مانند بیوپسی ساقه مغز مرتبط است.
🔰زمان عملیات نیز می تواند کوتاه شود. دکتر پارکر می گوید: «بیمار زمان کمتری را تحت بیهوشی می گذراند و بهبودی سریع تری دارد.
ممکن است افراد در مورد ماهیت دقیق جراحی رباتیک به مشاوره نیاز داشته باشند. دکتر پارکر میگوید: «بیماران اغلب فکر میکنند که یک ربات عمل جراحی را به تنهایی انجام میدهد – که در مورد محل قرار دادن الکترود فکر میکند. "اما این سیستم مستقل نیست. مانند یک بازوی فوق پایدار برای پزشکان است. ما کنترل می کنیم که کجا می رود، اما آن بازو بسیار روان تر و دقیق تر از دست یک جراح است.
گردآورنده : دکتر سمانه ظفرآبادی
مارا به دوستان خود معرفی کنید…🌱
🆔@NeurosurgeryAssociation
🆔@Neurosurgery_association
مقالات مرتبط
ویلیام گاورز
سر ویلیام گاورز، یک نورولوژیست برجسته در قرن نوزدهم، نقش اساسی در پیشبرد درک از اختلالات عصبی ایفا کرد. گاورز که در سال 1845 به دنیا آمد، از یک پیشینه متوسط بیرون آمد و سیر تحصیلی او، او را به دانشگاه کالج لندن هدایت کرد. او به عنوان پزشک مقیم در بیمارستان کالج لندن فعالیت کرد و بعد از آن، در سال ۱۸۷۰، اولین ثبت نام کننده در مرکز Queen Square شد و در نهایت در سال ۱۸۷۲ به عنوان پزشک کمکی افتخاری منصوب شد. گاورز به خاطر اخلاق کاری قابل توجه خود شناخته می شد و ساعات زیادی را به جنبه های مختلف عصب شناسی اختصاص می داد. مشارکت های او در این زمینه متنوع و تاثیرگذار بود. او «knee jerk» را به بالین بریتانیا معرفی کرد، که تکنیکی تشخیصی که در معاینات عصبی قابل توجه است. گاورز همچنین کمک های پیشگامی به درک اپیلپسی و بیماری های مزمن تشنجی کرد.
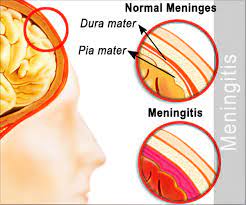
مننژیت
مننژیت باکتریال یک بیماری عفونی میباشد. بیمار مبتلا به مننژیت با تظاهراتی از قبیل شروع سردرد که اخیرا شروع شده باشد، تب، سفتی گردن، تغیر وضعیت هوشیاری مراجعه که حداقل دوتا از 4 تا تظاهر که نیازمند بررسی بالینی سریع میباشد. عوامل احتمالی مننژیت: 1)مننژیت نایسریا گنوره 2)مننژیت منگوکوکی 3)مننژیت استرپتوکوک پنومونیه 4)مننژیت لیستریا مونوسایتوژنز میباشد که هرکدام علایم منحصر به خود را دارند. ترجیح بر این است که درمان تجربی LPسریعتر اغاز شود تا از عوارض جبران ناپذیر این بیماری پیشگیری شود. انجام CT-scan تنها برای بیمارانی توصیه شده که یکی یا چندتا از علائم نشان دهنده افزایش فشار داخل مغز در انها وجود دارد.بررسی CSF در مواردی که تشخیص مننژیت سخت یا افتراق مننژیت باکتریال را از غیر باکتریالانجام میشود. کنتراندیکاسیون های انجام LP : اختلالات انعقادی، انعقاد داخل عروق منتشر، عفونت موضعی یا عدم یکپارچگی پوست در محل انجام LP میباشند.برای این بیماران در ابتدا دگزا متازون تزریق سپس ونکومایسن و سفتریاکسون اضافه میکنیم. بیماران در صورت داشتن ریسک فاکتور ها گفته شده برای باکتری لیستریا مونوسایتوژنز امپی سیلین و اگر شک مننژیت ویروسی ناشی از هرپس ویروس هم داشته باشیم میتوان اسیکلویر را به درمان گفته شده اضافه کرد.