مننژیوما
خلاصه مقاله
مننژیوما یکی ازتومورهای اولیه سیستم عصبی مرکزی است که در نخاع یا مغز بروز میکند و منشأ تومور از سلولهای مننژ و عنکبوتیه است. این تومور معمولاً خوشخیم است.تشعشعات یونیزان ، ریسک بیماری را از شش تا ده برابر بیشتر است. سندروم ارثی میتوانند زمینه را برای بروز مننژیوما فراهم کنند.مانند نوروفیبروماتوز نوع 2 (NF2) , Li-Fraumeni، Gorlin، von Hippel-Lindau، بیماری Cowden و نئوپلازی غدد درون ریز متعدد (تیپ1). هورمونهای جنسی بهعنوان عوامل خطر دیگر برای ایجاد مننژیوم مطرح میشوند. افزایش بروز بیماری پس از بلوغ در زنان (2:1 در مقابل مردان) و همچنین در طول دوره باروری (حدود 3:1) مطرح کننده این موضوع میباشد. ویژگی بافت شناسی پاتوگنومونیک مننژیوم، تشکیل whorls است که در نهایت به اجسام پساموما تبدیل می شوند. نشانگرهای ایمونوهیستوشیمی برای شناسایی مننژیوم عبارتند از: آنتی ژن غشای اپیتلیال، گیرنده سوماتوستاتین 2A، گیرنده پروژسترون و گیرنده استروژن ؛ آنتی ژن غشای اپیتلیال میباشد. WHO براساس ویژگی های هیستوپاتولوژیک: فعالیت میتوز ، تهاجم مغزی، و یا حداقل سه ویژگی تهاجمی دیگر مانند sheeting ، نسبت هسته به سیتوپلاسم بالا، هسته برجسته، سلولاریتی بالا و نکروز خود به خودی ، مننژیومها را طبقه بندی کرده و سه درجه بدخیمی را ذکر کرده است: مننژیوم های درجه یک می توانند طیف وسیعی از الگوهای بافت شناسی مختلف را ارائه دهند این الگوها عبارتند از: مننژوتلیال و فیبروز ، انتقالی، psammomatous,، angiomatous,، microcystic,، ترشحی، غنی از لنفوپلاسمیت و متاپلاستیک. از معیارهای طبقه بندی طیف درجه 1 : نرخ میتوز پایین، 4 در 10 HPFs و عدم تهاجم مغزی میتوان اشاره کرد. مننژیوم درجه 2 حداقل 3 ویژگی از ویژگی های زیر است: افزایش سلولاریتی، سلول های کوچک با نسبت بالای هسته به سیتوپلاسم، هسته برجسته، رشد مداوم بدون الگو یا رشد ورقه مانند، و کانون های نکروز خود به خود یا جغرافیایی. این طیفمی توانند بافت شناسی سلولی واضح و کوروئیدی داشته باشند. مننژیوم درجه 3 با ویژگی های بافتی بدخیمی تعریف میشود. چنین ویژگی هایی شامل سیتولوژی بدخیم (مانند ظاهری شبیه به سارکوم، کارسینوم یا ملانوم) یا شاخص میتوزی بالا است. زیرگروه هایی که دارای پتانسیل بیشتری برای تکثیر هستند، با درجه های II و III همراه هستند. اکثرا بدون علامت هستند ولی به محل درگیری ارتباط دارند. مننژیوم ها در تمام قسمت های جمجه یافت میشوند؛ خصوصا در ناحیه پاراساژیتال، و به دنبال آن فاکس، سینوس کاورنوس، توبرکلوم سلا، Lamina Cribrosa، تورامن مگنوم و Torcular Zones. علائمی همچون سردرد ، نقایص نورولوژیک کانونی یا تشنج عمومی و جزئی ، تیپیکال هستند. تغییرات شخصیتی، سردرگمی و تغییر سطح هوشیاری را میتوان مشاهده کرد و ممکن است به اشتباه به عنوان زوال عقل یا افسردگی تشخیص داده شود. مننژیوم های ستون فقرات اغلب در ناحیه توراسیک قرار دارند. هر فردی که اخیراً تشنج های او شروع شده یا علائم عصبی کانونی دارد که احتمال میرود با توده داخل جمجمه ارتباط داشته باشد، باید تحت تصویربرداری رزونانس مغناطیسی از مغز قرار گیرد. تشخيص آن راديولوژيك است و اگر تصويربرداري قویا حاكي از مننژيوم باشد، بيوپسي(روش تشخیص قطعی) اجباري نيست. در هر روش تصویربرداری، مننژیوم ها ویژگی های بسیار مشخصی را نشان می دهند که امکان تشخیص دقیق آنها را فراهم می کند و امروزه حتی سرنخ هایی برای تشخیص های بافت شناسی نیزارائه میدهند. بیشتر توده های کانونی و خارج محوری مننژیوم هستند و گاهی اوقات وجود جریان(شکاف) CSF در مجاورت تومور دیده می شود. تصویربرداری رزونانس مغناطیسی (MRI) روش استانداردی برای تشخیص رادیولوژیکی و نظارت بر مننژیوم است. میتوان از آن برای افتراق بین عود مننژیوم های تحت درمان با جراحی و تغییرات رادیولوژیک مرتبط با درمان (مانند ضخیم شدن دورا) استفاده کرد. در CT، کلسیفیکاسیون داخل ضایعه تغییرات استخوانی(هیپراستوز)، افزایش علائم عروقی و کلسیفیکاسیون پساموماتوز نیز دیده میشود. در اسکن های CT و MRI، مننژیوم ها به صورت بدون تکیه و یا ساقه دار(dural tail) با ظاهری ایزودنس و لکه مانند(به دلیل تشکیل عروق) دیده میشوند. مننژیوم خوش خیم دارای dural tail ضخیم و تقویت کننده کنتراست خواهد بود.نکروز مرکزی (hypointense T1، غیر تقویت کننده) را می توان در هر دو مننژیوم خوش خیم و بدخیم مشاهده کرد. درگیری عروق مغزی یک ویژگی شایع است، به ویژه برای مننژیوما های قاعده جمجمه، که ممکن است به شریان های کاروتید و بازیلار یا شاخه های آنها نزدیک شود. برای مننژیوم قاعده جمجمه، 18-fluoro-ethyl-tyrosine PET می تواند به تشخیص کمک کند. سایر تشخیصهای افتراقی شامل دیگر بیماریهای عفونی، التهابی یا نئوپلاستیک است که دورا یا فضای ساب دورال را درگیر میکنند، مانند متاستاز سایر تومورها، پلاسماسیتوما، لنفوم، تومور فیبری منفرد، گلیوسارکوم، سارکوئیدوز، گرانولوماتوز و سل. درمان 1)جراحی: برای تومورهای در حال رشد و علامت دار، استاندارد مراقبت یک رویکرد جراحی است. مکان نوروآناتومیک تومر، رویکرد جراحی را تعیین میکند؛ به طور مثال تومورهای پاراساژیتال ، با وجود سطحی بودن اما به دلیل درگیری سینوس ساژیتال ، پیچیده محسوب میشوند. تکنیکهای جدید جراحی شامل رویکردهای آندوسکوپی، جراحی هدایتشده با تصویر، مانیتورینگ عصبی، یا استفاده از ناوبری حین عمل و سیستمهای نوری است که امکان تجسم گستردهتر حین عمل را فراهم میکند. روش های آندوسکوپی از طریق حفره بینی برای درمان مننژیوم های موضعی در شیار بویایی، planum sphenoidale و tuberculum استفاده شده است.رادیوتراپی کمکی با هدف کاهش خطر عود و بهبود کنترل موضعی، مفید است. هنگامی که تومور برداشته می شود، از نوعی چسب برای جایگزینی دورا استفاده می شود. گسترش میزان برداشت(برش) از بافت با درجه سیمپسون اندازه گیری می شود و در پنج دسته قرار میگیرند: 1. برداشتن کامل، با برداشتن دورا و استخوان 2. برداشتن کامل کامل با انعقاد دورال 3. برداشتن ماکروسکوپی، بدون برش دورال یا انعقاد 4. برداشتن ساب توتال 5. بیوپسی جراحی می تواند عوارض عصبی، عصبی شناختی و عملکردی ایجاد کند و کیفیت زندگی این بیماران را محدود می کند. 2)پرتو درمانی: اگر برداشتن ساب توتال یا عوارض عمل جزء پیامدهای احتمالی باشد، باید به عنوان یک رویکرد درمانی اولیه در نظر گرفته شود. و برای کنترل رشد موضعی تومور استفاده میشود. در مننژیوم های درجه 1 در صورت برداشت ناقص در مناطق پرخطر مانند سینوس کاورنوس میتواند از رادیوتراپی استفاده کرد. در مننژیوم های درجه دو، نقش پرتودرمانی کمکی هنوز بحث برانگیز است، اما در موارد برداشت ناقص می توان آن را مد نظر قرار داد. مننژیوم درجه III با خطر بالاتر عود بعد از برداشتن همراه است، بنابراین رادیوتراپی با دوز بالا بعد از عمل استاندارد مراقبت است و با بهبود کنترل موضعی در ارتباط است. 3)درمان های سیستمیک: عوامل شیمی درمانی سیتوتوکسیک بررسی شده اثربخشی محدودی داشته اند و با دستورالعمل های اجماع توصیه نمی شوند.
مننژیوما:
مقدمه:
مننژیوم ها شایع ترین تومورهای اولیه داخل جمجمه ای است. علیرغم شهرت این تومور به عنوان یک بیماری کاملاً خوش خیم، مننژیوم اغلب با عوارضی مانند نقایص عصبی کانونی، تشنج و کاهش کیفیت زندگی همراه است. مننژیوم ها از سلول های عنکبوتیه واقع در سطح داخلی دورا منشأ می گیرند. در مرحله بعد، از سلول های پیشساز مننژ که از مزودرم و ستیغ عصبی مشتق شده، منشاء می گیرند. آنها می توانند در هر سطحی از دورای داخل جمجمه ای یا دورای نخاعی قرار بگیرند، اما گاهی اوقات می توانند در داخل بطن ها یا در اندام های خارج جمجمه ای (مانند ریه ها) نیز یافت شوند.
اپیدمیولوژی:
مننژیوم ها، 36.6 درصد از تومورهای اولیه CNS را تشکیل می دهند وشایع ترین تومورهای اولیه سیستم عصبی مرکزی به شمار میروند. بروز مننژیوم با افزایش سن به طور قابل توجهی افزایش مییابد، به گونه ای که از 0.14 در هر 100000 در کودکان 0-19 سال به 37.75 در هر 100000 در گروه سنی 75-84 سال افزایش می یابد. میانه سن تشخیص نیز 66 سال است. همچنین شیوع آن در بین زنان نسبت به مردان بیشتر است که این برتری تا حدی در ارتباط با سطح هورمونهای جنسی زنان است ؛ به گونه ای که حتی در سالهای باروری زنان نیز شیوع آن بیشتر میشود. مطالعات برتری شیوع مننژیوم در بین جمعیت سیاه پوستان را هم نشان میدهند.
عوامل خطر:
تشعشعات یونیزان به عنوان یکی از عوامل خطر شناخته میشوند، هرچند هم که رابطه واضحی بین دوز مواجهه و پاسخ آن وجود ندارد. با وجود این تشعشعات، ریسک بیماری را از شش تا ده برابر بیشتر است. مننژیوم های ناشی از تشعشع، اغلب متعدد هستند و تمایل به رفتار تهاجمی دارند.
چندین سندروم ارثی میتوانند زمینه را برای بروز مننژیوما فراهم کنند. شایع ترین علت ارثی که میتوان برای مننژیوم نام برد، نوروفیبروماتوز نوع 2 (NF2) است.(درواقع حذفی که بر ژن نوروفیبروماتوز نوع 2 اتفاق می افتد، یک اختلال اتوزومال غالب است که اغلب با حذف قابل مشاهده سیتوژنتیکی بازوی بلند کروموزوم 22 در q12 همراه است.) سایر سندروم ها عبارتند از : از Li-Fraumeni، Gorlin، von Hippel-Lindau، بیماری Cowden و نئوپلازی غدد درون ریز متعدد (تیپ1). تومورهای مرتبط با این شرایط اغلب متعدد بوده و شیوع آن در بین کودکان بیشتر است.
هورمونهای جنسی بهعنوان عوامل خطر دیگر برای ایجاد مننژیوم مطرح میشوند. افزایش بروز بیماری پس از بلوغ در زنان (2:1 در مقابل مردان) و همچنین با نسبت بالاتر بین زنان در طول دوره باروری (حدود 3:1) ادعای فوق را تایید میکنند. نشان داده شده است که تقریباً دو سوم تمام مننژیومها گیرندههای پروژسترون را بر روی غشای سلولی خود بیان میکنند. هرچند هم که علیرغم مطالعات انجام شده در این مورد ، هنوز شواهد قطعی وجود ندارد.
احتمال آسیب سر نیز برای القای مننژیوم وجود دارد، اما هنوز نمی توان به این سوال به طور قطع پاسخ داد. یک مکانیسم بالقوه، تغییر موضعی سد خونی مغزی به دلیل آسیب سر و در نتیجه هجوم گسترده سیتوکین ها، هیستامین و برادی کینین به فضای خارج عروقی است.
سیگار کشیدن، دیابت، فشار خون شریانی و استفاده از تلفن همراه نیز به عنوان عوامل خطر مورد بررسی قرار گرفته اند، اما نتایج قطعی نیست و تایید پاتولوژیک نیز ندارند.
هیستولوژِی:
ویژگی بافت شناسی پاتوگنومونیک مننژیوم، تشکیل اسفریکال سلول های مننژوتلیال به نام whorls است که در نهایت به اجسام پساموما تبدیل می شوند. tپاکسازی کروماتین مرکزی نیز در هستههای تومور همانند هجوم سیتوپلاسمی به هستهها که به شبه انکلوزیونهای سیتوپلاسمی داخل هستهای معروف هستند، رایج میباشد. با این حال، این ویژگی ها اغلب در بسیاری از مننژیوم ها نامحسوس هستند یا وجود ندارند. نشانگرهای ایمونوهیستوشیمی برای شناسایی مننژیوم عبارتند از: آنتی ژن غشای اپیتلیال، گیرنده سوماتوستاتین 2A، گیرنده پروژسترون (در 70-80٪ موارد وجود دارد) و گیرنده استروژن (در حدود 5-30٪ موارد وجود دارد)؛ که پرکاربردترین نشانگر، آنتی ژن غشای اپیتلیال میباشد. اگرچه مطالعات جدیدتر به وضوح نشان داده اند که گیرنده سوماتوستاتین 2A (SST2A) یک هدف برتر رنگ آمیزی ایمنولوژیکی است.
اکثر مننژیومها خوشخیم هستند اما میتوانند درجات متفاوتی از تمایززدایی را از خود نشان دهند. WHO براساس چندین ویژگی هیستوپاتولوژیک، از جمله فعالیت میتوز (تعداد میتوز در هر 10 میدان پرقدرت)، تهاجم مغزی، و یا حداقل سه ویژگی تهاجمی دیگر مانند sheeting (یعنی از دست دادن ساختار چرخشی یا فاسیکولار)، نسبت هسته به سیتوپلاسم بالا، هسته برجسته، سلولاریتی بالا و نکروز خود به خودی ، مننژیومها را طبقه بندی کرده و سه درجه بدخیمی را ذکر کرده است:
مننژیوم های درجه یک(80.5٪) می توانند طیف وسیعی از الگوهای بافت شناسی مختلف را ارائه دهند که امکان دارد از تومورهای دیگر نیز تقلید کنند. این الگوها عبارتند از: مننژوتلیال و فیبروز (که بیشترین فراوانی را دارند)، انتقالی، psammomatous,، angiomatous,، microcystic,، ترشحی، غنی از لنفوپلاسمیت و متاپلاستیک. از معیارهای طبقه بندی طیف درجه 1 میتوان به مواردی مثل : نرخ میتوز پایین، 4 در 10 HPFs و عدم تهاجم مغزی اشاره کرد.
تعریف مننژیوم درجه 2( آتیپیک،17.7% ) شامل افزایش فعالیت میتوزی یا دارا بودن حداقل 3 ویژگی از ویژگی های زیر است: افزایش سلولاریتی، سلول های کوچک با نسبت بالای هسته به سیتوپلاسم، هسته برجسته، رشد مداوم بدون الگو یا رشد ورقه مانند، و کانون های نکروز خود به خود یا جغرافیایی. این طیف از مننژیومها می توانند بافت شناسی سلولی واضح و کوروئیدی داشته باشند.
مننژیوم درجه 3(آناپلاستیک، کمتر از 2%) با ویژگی های بافتی بدخیمی که بسیار آشکارتر از ناهنجاری های موجود در مننژیوم آتیپیک است، تعریف میشود. چنین ویژگی هایی شامل سیتولوژی بدخیم (مانند ظاهری شبیه به سارکوم، کارسینوم یا ملانوم) یا شاخص میتوزی بالا (20 میتوز یا بیشتر در هر 10 HPF) است. تهاجم به مغز برای تشخیص مننژیوم آناپلاستیک کافی نیست. نشانه بافت شناسی در این طیف، پاپیلاری یا رابدوئید میباشد.
بیشتر مننژیومها، نئوپلاسمهای خوشخیم و با رشد آهسته هستند که از سلولهای کلاهکی (Cap cell) عنکبوتیه ناشی میشوند که به عنوان مننژیوم درجه یک در مقیاس درجهبندی WHO گروهبندی میشوند. زیرگروه هایی که دارای پتانسیل بیشتری برای تکثیر هستند، با درجه های II و III همراه هستند.
علائم:
اکثر مننژیوم ها بدون علامت هستند و بطور اتفاقی کشف می شوند. علائم آن مانند سایر تومورهای CNS، به محل درگیری ارتباط دارد. مننژیوم را می توان از هر سطح داخل جمجمه یا دورا نخاعی پیدا کرد. به ندرت، مننژیوم های داخل بطنی شناسایی می شوند. باتوجه به اینکه توزیع آناتومیکی مننژیومها با محل پرزهای عنکبوتیه موازی است، مننژیوم ها در تمام قسمت های جمجه یافت میشوند؛ خصوصا در ناحیه پاراساژیتال، و به دنبال آن فاکس، سینوس کاورنوس، توبرکلوم سلا، Lamina Cribrosa، تورامن مگنوم و Torcular Zones.
این تومرها ، رشد آهسته ای دارند و به ندرت infiltrative هستند. در حالی که هیچ تظاهرات پاتوگنومونیک مننژیوما وجود ندارد، اما علائمی همچون سردرد ناشی از افزایش فشار داخل جمجمه، نقایص نورولوژیک کانونی (از جمله اعصاب کرانیال) یا تشنج عمومی و جزئی ناشی از اثر توده فوکال، تیپیکال هستند. استفاده از پتانسیل معاینه عصبی بالینی، به تفسیر علائم مننژیوم و پیدا کردن محل آن کمک بسیاری کرده است. با این حال، در دسترس بودن تکنیکهای تصویربرداری مدرن، تشخیص مننژیوم را در مراحل اولیه تسهیل کرده است.
تغییرات شخصیتی، سردرگمی و تغییر سطح هوشیاری را می توان به ویژه در مننژیوم های قدامی (فرونتال) یا پاراساژیتال مشاهده کرد و ممکن است در ابتدا به اشتباه به عنوان زوال عقل یا افسردگی تشخیص داده شود.
مننژیوم های ستون فقرات اغلب در ناحیه توراسیک قرار دارند. هیپراستوز کانونی استخوان(نزدیک به تومور) یک یافته غیر معمول در مننژیوم است هرچند که مشخصه آن میباشد و تقریباً همیشه نشانه تهاجم استخوان توسط سلول های مننژیوما است.
تا به امروز هیچ روش غربالگری ثابتی برای مننژیوم وجود ندارد. عمل بالینی فعلی این است که هر فردی که اخیراً تشنج های او شروع شده یا علائم عصبی کانونی دارد که احتمال میرود با توده داخل جمجمه ارتباط داشته باشد، باید تحت تصویربرداری رزونانس مغناطیسی از مغز قرار گیرد.
از تشخیص های افتراقی آن میتوان به سایر ضایعات داخل جمجمه ای (مانند گلیوما یا تومورهای متاستاتیک) اشاره کرد.
تشخیص:
تشخيص آن راديولوژيك است و اگر تصويربرداري قویا حاكي از مننژيوم باشد، بيوپسي(روش تشخیص قطعی) اجباري نيست. در هر روش تصویربرداری، مننژیوم ها ویژگی های بسیار مشخصی را نشان می دهند که امکان تشخیص دقیق آنها را فراهم می کند و امروزه حتی سرنخ هایی برای تشخیص های بافت شناسی نیزارائه میدهند. بیشتر توده های کانونی و خارج محوری مننژیوم هستند و گاهی اوقات وجود جریان(شکاف) CSF در مجاورت تومور دیده می شود.
تصویربرداری رزونانس مغناطیسی (MRI) روش استانداردی برای تشخیص رادیولوژیکی و نظارت بر مننژیوم است.(در صورت عدم امکان استفاده ازMRI، میتوان از CT با کنتراست استفاده کرد). علاوه بر نقش MRI در تشخیص و نطارت بر مننژیوم، میتوان از آن برای افتراق بین عود مننژیوم های تحت درمان با جراحی و تغییرات رادیولوژیک مرتبط با درمان (مانند ضخیم شدن دورا) استفاده کرد.
در CT، کلسیفیکاسیون داخل ضایعه شایع است و نشانه های دیگری همچون تغییرات استخوانی(هیپراستوز)، افزایش علائم عروقی و کلسیفیکاسیون پساموماتوز نیز دیده میشود.
در اسکن های CT و MRI، مننژیوم ها به صورت بدون تکیه و یا ساقه دار(dural tail) با ظاهری ایزودنس و لکه مانند(به دلیل تشکیل عروق) دیده میشوند.
مننژیوم خوش خیم مشخصاً دارای dural tail ضخیم و تقویت کننده کنتراست خواهد بود. لازم به ذکر است، dural tail برای مننژیوما پاتگنومونیک نیست و ممکن است در متاستازها یا همانژیوپریسایتوما نیز دیده شود، اما اغلب در تشخیص مننژیوم از سایر ضایعات (مانند شوانوما که در آن وجود ندارد)، مفید است.
نکروز مرکزی (hypointense T1، غیر تقویت کننده) را می توان در هر دو مننژیوم خوش خیم و بدخیم مشاهده کرد.
درگیری عروق مغزی یک ویژگی شایع است، به ویژه برای مننژیوما های قاعده جمجمه، که ممکن است به شریان های کاروتید و بازیلار یا شاخه های آنها نزدیک شود. برای مننژیوم قاعده جمجمه، 18-fluoro-ethyl-tyrosine PET می تواند به تشخیص کمک کند، اما اطلاعاتی در مورد بافت شناسی ارائه نمی دهد.
سایر تشخیصهای افتراقی شامل دیگر بیماریهای عفونی، التهابی یا نئوپلاستیک است که دورا یا فضای ساب دورال را درگیر میکنند، مانند متاستاز سایر تومورها، پلاسماسیتوما، لنفوم، تومور فیبری منفرد، گلیوسارکوم، سارکوئیدوز، گرانولوماتوز و سل.
درمان:
1)جراحی:
برای بسیاری از بیمارانی که با مننژیوم، به ویژه تومورهای بدون علامت مراجعه می کنند، نظارت رادیولوژیک به تنهایی یک استراتژی قابل قبول است. درحالیکه برای تومورهای در حال رشد و علامت دار، استاندارد مراقبت یک رویکرد جراحی است. باید توجه داشت ممکن است توانایی دستیابی به برداشت کامل تومور توسط تعدادی ازعوامل، از جمله محل تومور محدود شود. مکان نوروآناتومیک تومر، رویکرد جراحی را تعیین میکند؛ به طور مثال تومورهای پاراساژیتال ، با وجود سطحی بودن اما به دلیل درگیری سینوس ساژیتال ، پیچیده محسوب میشوند. تکنیکهای جدید جراحی شامل رویکردهای آندوسکوپی، جراحی هدایتشده با تصویر، مانیتورینگ عصبی، یا استفاده از ناوبری حین عمل و سیستمهای نوری است که امکان تجسم گستردهتر حین عمل را فراهم میکند. روش های آندوسکوپی از طریق حفره بینی برای درمان مننژیوم های موضعی در شیار بویایی، planum sphenoidale و tuberculum استفاده شده است. پیشرفت در درمان مننژیوم انعکاسی از پیشرفت های جراحی مغز و اعصاب است که حداکثر استفاده را برای بهبود درمان به کار می برد. این نکته نیز بسیار اهمیت دارد که هرچه برداشتن تومور کامل تر باشد، فرصت عود کمتر و شانس درمان بیشتر است. پس از جراحی، رادیوتراپی کمکی با هدف کاهش خطر عود و بهبود کنترل موضعی، مفید است.
هنگامی که تومور برداشته می شود، از نوعی چسب برای جایگزینی دورا استفاده می شود. در موارد درگیری استخوان، که می تواند محل عود را نشان دهد، این قسمت ها هم باید برداشته شوند. گسترش میزان برداشت(برش) از بافت با درجه سیمپسون اندازه گیری می شود و در پنج دسته قرار میگیرند:
1. برداشتن کامل، با برداشتن دورا و استخوان
2. برداشتن کامل کامل با انعقاد دورال
3. برداشتن ماکروسکوپی، بدون برش دورال یا انعقاد
4. برداشتن ساب توتال
5. بیوپسی
باید توجه داشت که متأسفانه جراحی می تواند عوارض عصبی، عصبی شناختی و عملکردی ایجاد کند و کیفیت زندگی این بیماران را محدود می کند.
2)پرتو درمانی:
روش دیگر، رادیوتراپی است که اگر برداشتن ساب توتال یا عوارض عمل جزء پیامدهای احتمالی باشد، باید به عنوان یک رویکرد درمانی اولیه در نظر گرفته شود. برای چندین دهه، پرتودرمانی (RT) درمان اولیه برای تومورهای در حال رشد بدون نیاز به جراحی بوده است. باید توجه داشت که RT به اندازه جراحی، در تسکین علائم عصبی مرتبط با تومور موفق نیست. با این حال، برای بیمارانی که تومورهای آنها از نظر جراحی غیرقابل دسترس است، RT اغلب برای کنترل رشد موضعی تومور استفاده میشود.روشهای مختلف رادیوتراپی را می توان در محیط کمکی پس از برداشتن تومر با جراحی یا برای درمان عود بیماری استفاده کرد: رادیوتراپی با پرتو خارجی (EBRT) و single-fraction stereotactic radiosurgery (SRS).
Single-fraction SRS معمولاً در مننژیوم هایی با قطر کمتر از 30 میلی متر که در مجاورت ساختارهای حساس به تشعشع نیستند استفاده می شود.
استفاده از رادیوتراپی کمکی در مننژیوم های درجه 1 که با استفاده از جراحی به طور کامل برداشته شده اند، قابل اجتناب است. اما در صورت برداشت ناقص در مناطق پرخطر مانند سینوس کاورنوس میتواند از رادیوتراپی استفاده کرد. در مننژیوم های درجه دو، نقش پرتودرمانی کمکی هنوز بحث برانگیز است، اما در موارد برداشت ناقص می توان آن را مد نظر قرار داد. مننژیوم درجه III با خطر بالاتر عود بعد از برداشتن همراه است، بنابراین رادیوتراپی با دوز بالا بعد از عمل استاندارد مراقبت است و با بهبود کنترل موضعی در ارتباط است.
3)درمان های سیستمیک:
استفاده از درمانهای سیستمیک در مننژیومها با توجه به نتایج محدود ، تا حد زیادی تجربی باقی مانده و در موارد بیماری عودکننده/پیشرونده که برای جراحی یا رادیوتراپی مناسب نیستند، اختصاص دارد. در حال حاضر شواهد روشنی در مورد استاندارد مراقبت وجود ندارد. عوامل شیمی درمانی سیتوتوکسیک بررسی شده اثربخشی محدودی داشته اند و با دستورالعمل های اجماع توصیه نمی شوند.
چندین ترکیب در مطالعات مختلف مورد بررسی قرار گرفتهاند، مانند IFN-α، آنالوگهای سوماتوستاتین (pasireotide و octreotide)، مهارکنندههای VEGF/VEGFR، مهارکنندههای EGFR(erlotinib و gefitinib)، imatinib، mifepristone و شیمی درمانی(hydroxyurea, temozolomide, irinotecan و trabectedin). برخی مطالعات اثربخشی آلفا اینترفرون و عوامل ضد رگ زایی که VEGF را هدف قرار می دهند را نشان داده است.
پیش آگهی:
سابقه طبیعی تومورهای درجه II و درجه III بسیار تهاجمی تر است (با نرخ عود در 5 سال تقریباً 50٪ برای تومورهای درجه II و 90٪ برای تومورهای درجه III). این تکرارها به مرگ و میر اختصاصی مننژیوما در این بیماران، با نرخ بقای کلی 10 ساله 53٪ برای بیماران درجه II و 0٪ برای بیماران درجه III، علیرغم تلاش های درمانی تهاجمی، منجر میشود.اصطلاح پیشرفت در بحث مننژیوم برای توصیف رشد تومور باقی مانده استفاده می شود. همچنین می تواند برای توصیف تبدیل از یک تومور درجه پایین به یک تومور با درجه بالاتر استفاده شود. اگرچه اغلب به دنبال درمان غیرجراحی با پرتودرمانی، ثبات (عدم رشد) وجود دارد، اما مننژیوما ها به ندرت کاهش اندازه را در پاسخ رادیوگرافی نشان می دهند. استراتژیهای مختلفی برای ارزیابی رشد تومور ارزیابی شده است، مانند رشد 2 بعدی خطی ،رشد 3 بعدی حجمی، سرعت رشد؛ اما هیچ کدام استاندارد نیست
مقالات مرتبط
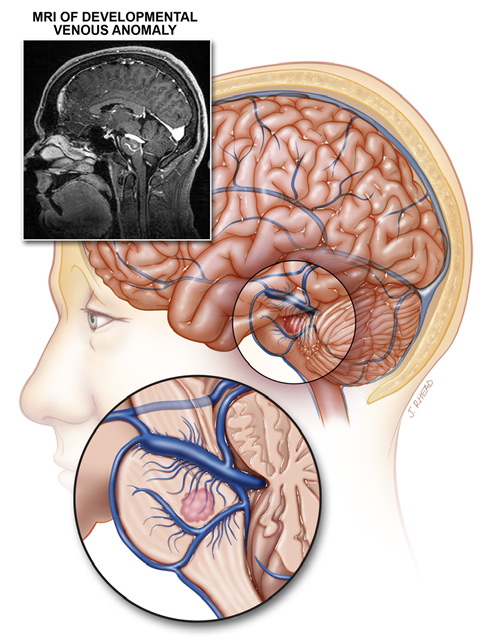
آنومالی مادرزادی وریدی دستگاه عصبی Develompental Venous Anomaly
ناهنجاری های تکاملی وریدی نوعی ضایعه شایع هستند که در آن ها، وریدهایی که در حالت طبیعی به صورت شعاعی قرار دارند با هم تلاقی نموده و تبدیل به یک کانال وریدی متسع می شوند. DVA شایعترین ناهنجاری عروقی مغزی رویت شده در اتوپسی بوده و بطور معمول بصورت تصادفی در تصویربرداری یافت می شوند. DVA معمولا خوش خیم است اما در مواردی ممکن است موجب پاتولوژی ایسکمیک یا هموراژیک شود.
جراحی مغز و اعصاب عملکردی چیست؟ Functional Neurosurgery
جراحی مغز و اعصاب عملکردی یکی از فلوشیپ های جراحی اعصاب است