مطالعه آزمایشگاهی پاتوژنز پیشرفت MS را روشن می کند
خلاصه مقاله
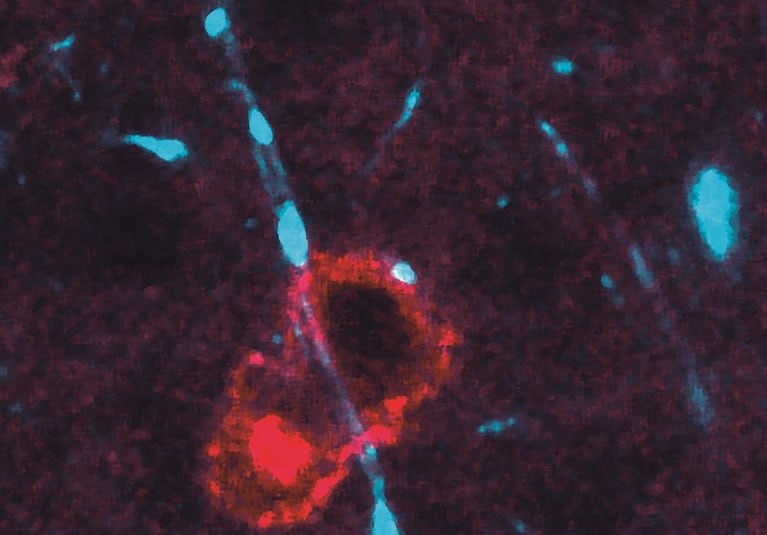
مکانیسم های بیماری زایی که باعث پیشرفت بیماری در مولتیپل اسکلروزیس (MS) می شود، مشخص نشده است. یک مطالعه کلینیک مایو شواهدی را ارائه می دهد که سلول های neuroantigen-specific T cellsبه بخش های دمیلینه شده سیستم عصبی مرکزی نفوذ می کنند و باعث از بین رفتن نورون و پیشرفت بیماری می شوند.
#خبرنامه
#مطالعه_پاتوژنز_ام_اس
مطالعه آزمایشگاهی پاتوژنز پیشرفت MS را روشن می کند
🔰 مکانیسم های بیماری زایی که باعث پیشرفت بیماری در مولتیپل اسکلروزیس (MS) می شود، مشخص نشده است. یک مطالعه کلینیک مایو شواهدی را ارائه می دهد که سلول های neuroantigen-specific T cellsبه بخش های دمیلینه شده سیستم عصبی مرکزی نفوذ می کنند و باعث از بین رفتن نورون و پیشرفت بیماری می شوند.
🔰 محققان از مدل های آزمایشگاهی MS برای بررسی پاتوژنز پیشرفت MS استفاده کردند. این مطالعه در Journal of Clinical Investigation منتشر خواهد شد.
🔰 یافته های کلیدی:
1-دمیلیناسیون منجر به ارائه یک نئوآنتی ژن اختصاصی نورون به سلول های CD8+ T اختصاصی آنتی ژن شد.
2-در محیط دمیلیناسیون، سلول های CD8 + T تکثیر شده و به نورون ها و آکسون ها آسیب می رساند.
3-زمانی که دمیلیناسیون وجود نداشته باشد، سلول های ایمنی می توانند وارد سیستم عصبی مرکزی (که شامل مغز، اعصاب بینایی و نخاع می شود) شوند و به گشت زنی بپردازند، اما برای مدت طولانی در آنجا باقی نمی مانند. به عبارت دیگر آنها آسیب زیادی به نورون ها و آکسون ها وارد نمی کنند، مگر اینکه دمیلیناسیون وجود داشته باشد.
🔰 محققان دریافتند که سلولهای عصبی مغز و نخاع افرادی که به دلیلMS جان خود را از دست دادهاند، رونوشتهای MHC کلاس 1 و پروتئینهای بیشتری نسبت به حالت عادی دارند. این نشان میدهد که سلولهای CD8+ T که میتوانند این سلولها را شناسایی و از بین ببرند، در ایجاد MS و بدتر شدن آن نقش دارند.
🔰 ( توضیح بیشتر: محققان دریافتند که نورون های مغز و نخاع افراد مبتلا به MS، پروتئین MHC کلاس 1 بیشتری را نسبت به حالت عادی بیان می کنند. این نشان میدهد که سلولهای CD8+ T ممکن است به نورونها و آکسونها حمله کنند که خود میتواند در پیشرفت MS نقش داشته باشد.)
لینک خبر
گرد آورنده: دکتر محمد سینا میرجانی
مارا به دوستان خود معرفی کنید…🌱
🆔@NeurosurgeryAssociation
🆔@Neurosurgery_association
مقالات مرتبط
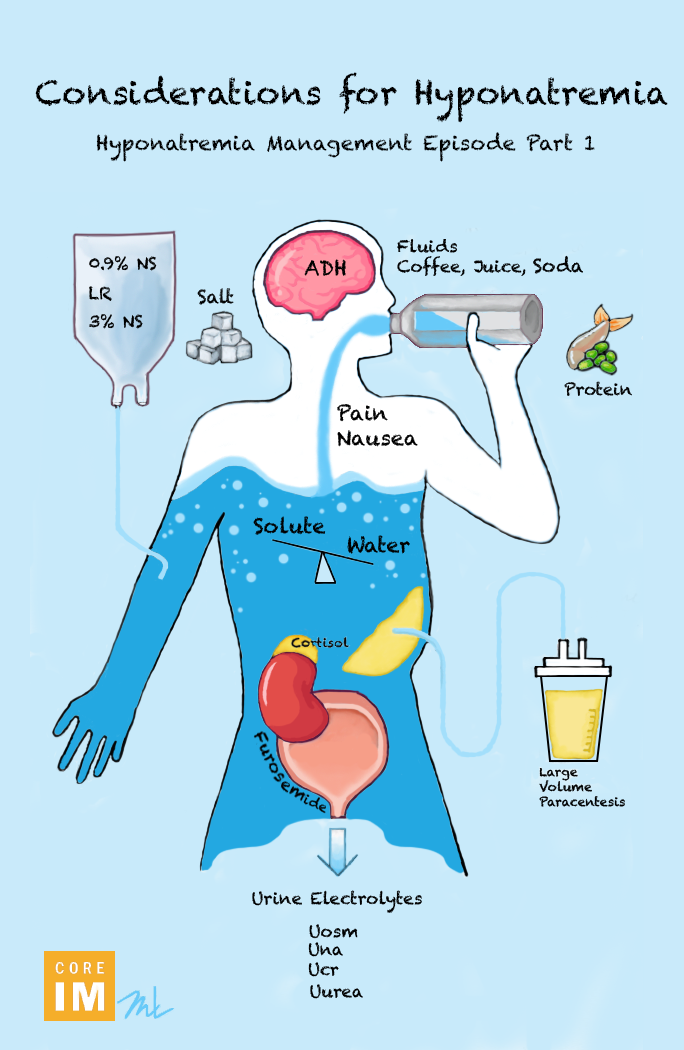
هرآنچه در مدیریت هایپوناترمی مهم است.
هایپوناترمی شرایط خطرناکی است که در بیماران بویژه بیماران جراحی مغز و اعصاب بسیار خطرناک است.
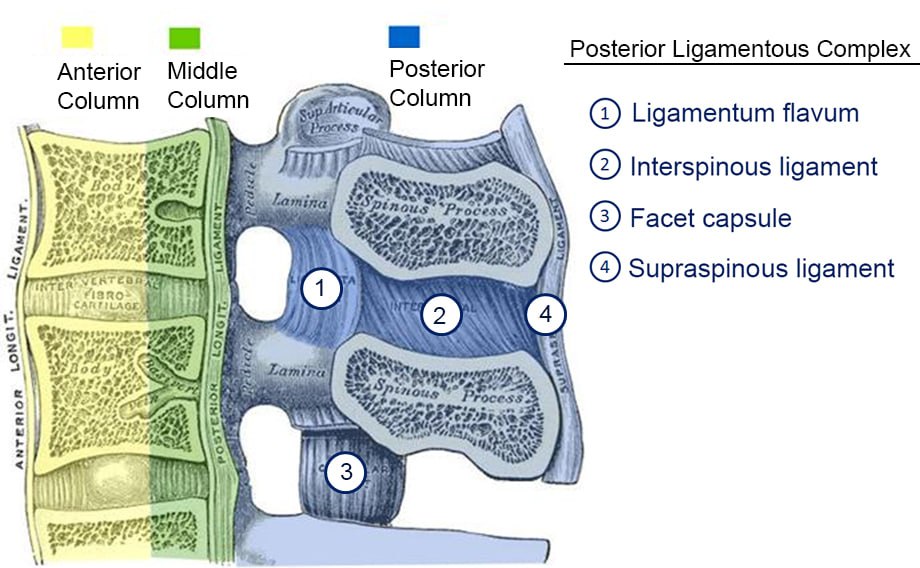
سندرم طناب خلفی
سندرم طناب خلفی نوع نادری از آسیب ناقص نخاعی با شیوع 1٪ است که بر ستونهای پشتی نخاع تأثیر میگذارد که مسئول درک لمس ظریف، ارتعاش، احساس خود حرکتی و موقعیت بدن (حس عمقی) هستند.