بررسی روند تشخیص آلزایمر و آسیب شناسی این بیماری؛ ( از بکارگیری روشهای تصویربرداری تا استفاده از بیومارکرها)
خلاصه مقاله
در تشخیص آلزایمر امروزه وابسته به شرایط بالینی، تصویربرداری و نیز امروزه، روش های بیولوژیک هم کارایی دارد
#Neuro_AI
📱عنوان مقاله: بررسی روند تشخیص آلزایمر و آسیب شناسی این بیماری؛ ( از بکارگیری روشهای تصویربرداری تا استفاده از بیومارکرها)
🔰مقدمه و تاریخچه
بیماری آلزایمر (AD) که به نام آلوئیس آلزایمر روانپزشک آلمانی نام گرفته است، شایع ترین نوع زوال عقل است. این بیماری می تواند به عنوان یک بیماری تخریب کننده عصبی به آرامی پیشرونده تعریف شود که با پلاک های عصبی و گره های نوروفیبریلار در نتیجه تجمع (Aβ) پپتید آمیلوئید بتا در آسیبدیدهترین ناحیه مغز، لوب تمپورال میانی و ساختارهای نئوکورتیکال مشخص می شود.
به عنوان تاریخچه باید بیان نمود که آلوئیس آلزایمر هنگام بررسی مغز اولین بیمار خود که قبل از مرگ دچار از دست دادن حافظه و تغییر شخصیت شده بود، متوجه وجود پلاک های آمیلوئید و از دست دادن گسترده نورون ها شد و این وضعیت را یک بیماری جدی قشر مغز توصیف کرد. این وضعیت پزشکی برای اولین بار بیماری آلزایمر نامیده شد [کریپلین، ا.، کتاب راهنمای روانپزشکی، ویرایش هشتم]. از دست دادن پیشرونده عملکردهای شناختی می تواند ناشی از اختلالات مغزی مانند بیماری آلزایمر (AD) یا عوامل دیگری مانند مسمومیت ها، عفونت ها، ناهنجاری در سیستم ریوی و گردش خون باشد که باعث کاهش اکسیژن رسانی به مغز، کمبود تغذیه، کمبود ویتامین B12، تومورها و موارد دیگر می شود.
🔰در حال حاضر، حدود 50 میلیون بیمار AD در سراسر جهان وجود دارد و پیش بینی می شود که این تعداد هر 5 سال دو برابر شود و تا سال 2050 به 152 میلیون نفر افزایش یابد. در حال حاضر، هیچ درمانی برای بیماری آلزایمر وجود ندارد، اگرچه درمانهایی در دسترس هستند که فقط علائم را بهبود میبخشند.
هدف اصلی از این بررسی، ارائه توضیحات مختصری در مورد تشخیص، آسیب شناسی، علل و درمان های فعلی AD و برجسته کردن پیشرفت اخیر ترکیباتی است که می توانند با هدف قرار دادن چندین مکانیسم بیماری زا، مانند Aβ و tau aggregation، و میس فولدینگ (misfolding)، التهاب، آسیب اکسیداتیو، و غیره از AD جلوگیری یا آن را درمان کنند.
🔰تشریح و بررسی معیارهای بدست آمده برای تشخیص بیماری
۱- معیارهای تشخیصی بیماری آلزایمر
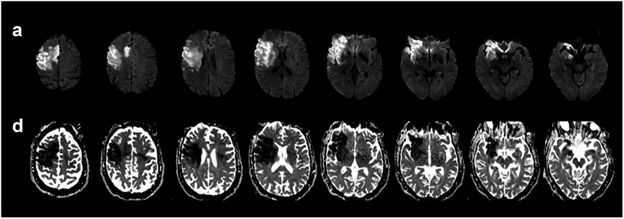
در بیمار مشکوک به AD باید آزمایش های متعددی از جمله معاینه عصبی، تصویربرداری تشدید مغناطیسی (MRI) برای نورون ها، معاینات آزمایشگاهی مانند ویتامین B12 و سایر آزمایشات غیر از سابقه پزشکی و خانوادگی بیماران را انجام دهد . بر اساس برخی مطالعات، کمبود ویتامین (ویتامین B12) مدتهاست که به دلیل ارتباط آن با مشکلات عصبی و افزایش خطرات AD شناخته شده است. نشانگر ویژه کمبود B12 افزایش سطح هموسیستئین است که می تواند باعث آسیب مغزی در اثر استرس اکسیداتیو، افزایش هجوم کلسیم و آپوپتوز شود. تشخیص های ویتامین. کمبود B12 را می توان با اندازه گیری ویتامین سرم انجام داد.
در سال 1984، موسسه ملی اختلالات عصبی و ارتباطی و سکته مغزی (NINCDS) و انجمن بیماری آلزایمر و اختلالات مرتبط (ADRDA) یک گروه کاری (NINCDS-ADRDA) را برای ایجاد معیارهای تشخیصی بالینی برای بیماری آلزایمر تشکیل دادند. این معیارها شامل موارد زیر است: (1-1) بیماری احتمالی آلزایمر، که در آن زوال عقل با آزمایشهای عصبی روانشناختی تأیید میشود، از دست دادن پیشرونده حافظه، اختلال در فعالیتهای روزمره زندگی، و سایر علائم مانند آفازی (اختلال زبان)، آپراکسی (حرکتی)، اختلال مهارت ها و آگنوزیا (از دست دادن ادراک) تشخیص داده می شود. همه این علائم ممکن است از سن 40 تا 90 سالگی و بدون وجود هر گونه بیماری سیستمیک یا مغزی ظاهر شوند،
(2-1) بیماری احتمالی آلزایمر را می توان در غیاب اختلالات عصبی، روانپزشکی و وجود بیماری دیگری مانند بیماری سیستمیک یا مغزی اعمال کرد. اما آنها علت اولیه زوال عقل نیستند،
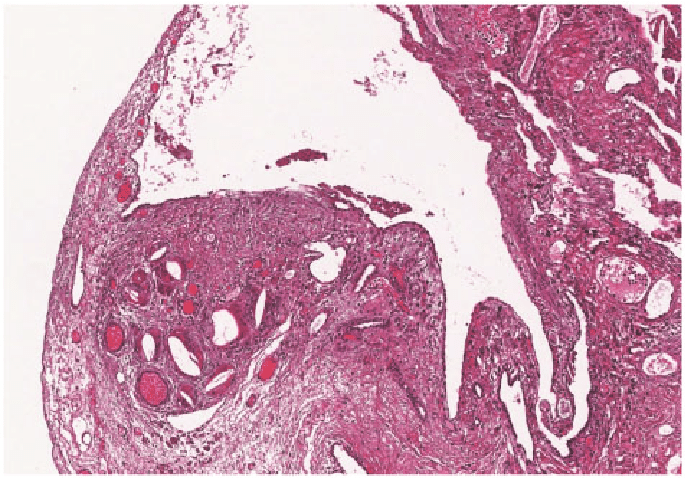
(3-1) بیماری قطعی آلزایمر، که با تایید هیستوپاتولوژیک به دست آمده از بیوپسی یا کالبد شکافی تایید می شود.
در سال 2011، چندین تغییر در معیارهای قبلی ایجاد شد [موسسه ملی پیری-آلزایمر، ۲۰۱۱] و معیارهای NINCDS-ADRDA 1984 برای ویژگی و حساسیت بالاتر در تشخیص بیماری آلزایمر به روز شد.
🔰معیارهای پیشنهادی جدید شامل زوال عقل احتمالی برای استفاده در محیط های بالینی و زوال عقل احتمالی یا احتمال AD با شواهد پاتوفیزیولوژیکی برای اهداف تحقیقاتی، علاوه بر نشانگرهای زیستی بالینی است. دو دسته از بیومارکرهای بیماری آلزایمر وجود دارد: (الف) نشانگرهای آمیلوئید مغز مانند توموگرافی انتشار پوزیترون (PET) و مایع مغزی نخاعی (CSF)،
🔰بررسی روند تشخیص آلزایمر
دو نوع تغییر نوروپاتولوژیک در AD وجود دارد که شواهدی را در مورد پیشرفت بیماری و علائم آن ارائه می دهد. این تغییرات شامل:
(1) ضایعات مثبت است که با تجمع گره های نوروفیبریلاری، پلاک های آمیلوئید، نوریت های دیستروفیک و رشته های نوروپیل مشخص می شود.
(۲) ضایعات منفی که با آتروفی بزرگ به واسطه از دست دادن سلول های عصبی، نوروپیل و سیناپس ها مشخص می شود. علاوه بر این، عوامل دیگری مانند التهاب های نورونی، استرس اکسیداتیو و آسیب نورون های کولینرژیک می توانند باعث تخریب عصبی شوند.
🔰 پلاک های سالخوردگی
پلاک های پیری رسوبات خارج سلولی پروتئین بتا آمیلوئید (Aβ) با اشکال مورفولوژیکی مختلف از جمله پلاک های عصبی به شکل هسته های متراکم یا فشرده هستند. آنزیم های پروتئولیتیک مانند β-سکرتاز و γ-سکرتاز مسئول بیوسنتز رسوبات Aβ از پروتئین پیش ساز آمیلوئید (APP) هستند. این آنزیم ها APP را به چند قطعه آمینو اسید تقسیم می کنند: اسیدهای آمینه 43، 45، 46، 48، 49 و 51 که به فرم های نهایی Aβ40 و Aβ42 می رسند. انواع مختلفی از مونومرهای Aβ وجود دارد، از جمله فیبریل های آمیلوئیدی بزرگ و نامحلول که می توانند برای تشکیل پلاک های آمیلوئید و الیگومرهای محلول که می توانند در سراسر مغز پخش شوند تجمع کنند. Aβ نقش عمدهای در سمیت عصبی و عملکرد عصبی دارد، بنابراین تجمع پلاکهای متراکمتر در هیپوکامپ، آمیگدال و قشر مغز میتواند باعث تحریک آستروسیتها و میکروگلیا، آسیب به آکسونها، دندریتها و از دست دادن سیناپسها و همچنین اختلالات شناختی شود.
🔰گره های عصبی فیبریلاری (NFTs)
رشتههای غیرطبیعی پروتئین هیپرفسفریله شده هستند که در برخی مراحل میتوانند به دور یکدیگر پیچ خورده و رشتههای مارپیچ زوجی (PHF) را تشکیل دهند و در سیتوپلاسم عصبی پریکاریال، آکسونها و دندریتها تجمع کنند که باعث از بین رفتن میکروتوبولهای اسکلت سلولی و توبولینهای پروتئینی میشوند. پروتئین تاو هیپرفسفریله، ماده اصلی تشکیل دهنده NFT در مغز بیماران مبتلا به AD است و تکامل آن می تواند منعکس کننده مراحل مورفولوژیکی NFT باشد، که عبارتند از: (۱) فاز پیش از گره خوردن، یک نوع NFT، که در آن پروتئین های تاو فسفریله در انباشته می شوند. محفظه سوماتودندریتیک بدون تشکیل PHF، (۲) NFT های بالغ، که با تجمع رشته ای پروتئین تاو با جابجایی هسته به قسمت پیرامونی سوما مشخص می شوند، و (3) گره های خارج سلولی، یا مرحله NFT های شبح که ناشی از از دست دادن نورون به دلیل مقادیر زیاد پروتئین تاو رشته ای با مقاومت نسبی در برابر پروتئولیز است.
🔰از دست دادن سیناپسی
آسیب سیناپسی در نئوکورتکس و سیستم لیمبیک باعث اختلال در حافظه می شود و به طور کلی در مراحل اولیه AD مشاهده می شود. مکانیسمهای از دست دادن سیناپسی شامل نقص در حمل و نقل آکسونی، آسیب میتوکندری، استرس اکسیداتیو و سایر فرآیندهایی است که میتوانند به بخشهای کوچکی مانند تجمع Aβ و تاو در مکانهای سیناپسی کمک کنند. این فرآیندها در نهایت منجر به از بین رفتن خارهای دندریتیک، پایانه های پیش سیناپسی و دیستروفی آکسون می شوند. پروتئین های سیناپسی به عنوان نشانگرهای زیستی برای تشخیص از دست دادن و شدت سیناپس ها مانند نوروگرانین، پروتئین عصبی پس سیناپسی، پروتئین شبه ویزینین-1 (VILIP-1) و سیناپتوتاگمین-1 عمل می کنند.
🔰مراحل بیماری آلزایمر
مراحل بالینی بیماری آلزایمر را می توان به مراحلی تقسیم نمود:
(۱) مرحله پیش بالینی یا پیش علامتی طبقه بندی کرد که می تواند چندین سال یا بیشتر طول بکشد. این مرحله با از دست دادن حافظه خفیف و تغییرات پاتولوژیک اولیه در قشر و هیپوکامپ، بدون اختلال عملکردی در فعالیتهای روزانه و عدم وجود علائم و نشانههای بالینی AD مشخص میشود. ۲- مرحله خفیف یا اولیه بیماری AD، که در آن علائم متعددی در بیماران ظاهر می شود، مانند مشکل در زندگی روزمره بیمار با از دست دادن تمرکز و حافظه، بی نظمی مکان و زمان، تغییر در خلق و خو. ، و توسعه افسردگی. ۳- مرحله متوسط AD، که در آن بیماری به نواحی قشر مغز گسترش می یابد که منجر به افزایش از دست دادن حافظه با مشکل در شناخت خانواده و دوستان، از دست دادن کنترل تکانه و مشکل در خواندن، نوشتن و صحبت می شود. ۴- AD شدید یا در اواخر مرحله، که شامل گسترش بیماری به کل ناحیه قشر با تجمع شدید پلاکهای عصبی و درهمتنیدگیهای نوروفیبریلاری است که منجر به یک اختلال عملکردی و شناختی پیشرونده میشود که در آن بیماران به هیچ وجه نمیتوانند خانواده خود را بشناسند و ممکن است با مشکل در بلع و ادرار در بستر شود و در نهایت به دلیل این عوارض منجر به مرگ بیمار شود.
گردآورنده: دکتر علیرضا اعرابی
مقالات مرتبط
سکته_مغزی
سکته مغزی یکی از علل اصلی مرگ و ناتوانی میباشد. شایعترین اختلالات عصبی-روانی مرتبط با سکته شامل افسردگی، اضطراب، ناپایداری عاطفی، اختلالات ارتباط عاطفی و بیتفاوتی هستند
سیستم های رباتیک جراحی های استریوتاکتیک پیچیده را تسهیل می کنند
سیستم های رباتیک جراحی های استریوتاکتیک پیچیده را تسهیل می کنند